تلعب إشارات المركبات الريتينويدية دورًا أساسيًا أثناء تطور الجنين في الرحم، ولها أهمية خاصة في تكون الجهاز العصبي. الريتينويدات Retinoids هي مستقلبات فيتامين أ في الجسم، وتؤثر على التعبير عن آلاف عمليات نسخ الجينوم، وبذلك تعمل بمثابة منظم رئيسي للعديد من العمليات البيولوجية المهمة.
مقدمة
الفصام أو الشيزوفرينيا Schizophrenia هو اضطراب نفسي، يتأثر بمجموعة من العوامل الوراثية والبيئية، لكن ما زالت معالجة المرض صعبة، والتقدم في مجال العلاج طفيف جدًا.
يتضمن العلاج الحالي مضادات الذهان Anti-Psychotic التقليدية، ولأن الآلية المرضية معقدة، فإن تطوير العلاجات الجديدة المحتملة صعب، إذ تتوقف طبيعة المرض بدرجة كبيرة على المريض نفسه، وتركيبه الوراثي، والتعرض للإجهاد الجسدي أو النفسي أو الاجتماعي، ما يتفق مع فرضية التطور العصبي طويل الأمد للفصام، إذ يؤثر التفاعل بين العوامل البيئية والجينية على التطور العصبي المبكر، ويتوافق ذلك مع انخفاض حجم التغصنات العصبية Dendritic Volume، وكثافتها، والتي تُلاحظ مجهريًا في صورة رقة القشرة الدماغية، ونقص الاتصال العصبي.
ارتكزت الأبحاث المبكرة على فرضية دور الدوبامين في الدماغ، نظرًا لدوره الواضح في المرض، ولكن اتضح لنا بعد ذلك وجود العديد من المسارات الحيوية الأخرى المرتبطة بالفصام والاضطرابات الذهانية الأخرى.
ولذلك يجب أن تبدأ معالجة المرض بحل المشاكل الموجودة في هذه المسارات الحيوية، خاصةً تلك التي يمكن معالجتها عن طريق الأدوية، وهنا يتضح لنا أهمية نظام تصنيع الريتينويدات، الذي سيمثل منافسًا قويًا في مجال معالجة مرض الفصام، بسبب دوره المهم في التحكم في التطور العصبي، اعتمادًا على التحكم في التمايز الخلوي العصبي Neuronal Differentiation.
الريتينويدات هي مستقلبات فيتامين أ (الريتينول Retinol)، وهو فيتامين ذائب في الدهون، يُشتق من الأطعمة في صورته النشطة، أو في صورة أسلاف أولية Provitamin Precursors للفيتامين مثل بيتا كاروتين، وللريتيونيدات تأثيرات عديدة جينية وغير جينية.
فإلى جانب دورها في نمو الجنين، تلعب دورًا مهمًا أيضًا في عمليات أخرى تحدث بعد الولادة، مثل لدونة التشابك العصبي Synaptic Plasticity، وتكوّن الخلايا اللمفاوية، والالتهاب، والدورة الإبصارية، وتتميز هذه التغيرات بالتأثر بالناهضات Agonists والمضادات Antagonists الطبيعية والصناعية للريتينويدات، ما يجعلها هدفًا مفترضًا للعديد من العلاجات.
نظام نقل الريتينويدات
تُخزن أكثر الريتينويدات في الكبد في صورة إسترات الريتينيل Retinyl Esters، والناقل الأساسي للريتينول في الدم هو البروتين الرابط للريتينول 4RBP. تفرز الخلايا الكبدية الريتينول إلى البلازما مرتبطًا مع البروتين RBP4 ، ليرتبط بدوره بترانس ثيريتين رباعي البروتين TTR، مكونًا معقد Complex.
بعد ارتباطه بالبروتين RBP4 المرتبط بالريتينول، ينظم البروتين TTR تركيز الريتينول في الدم، عن طريق التحكم في الترشيح الكلوي للبروتين RBP4.
[caption id="attachment_76321" align="aligncenter" width="511"]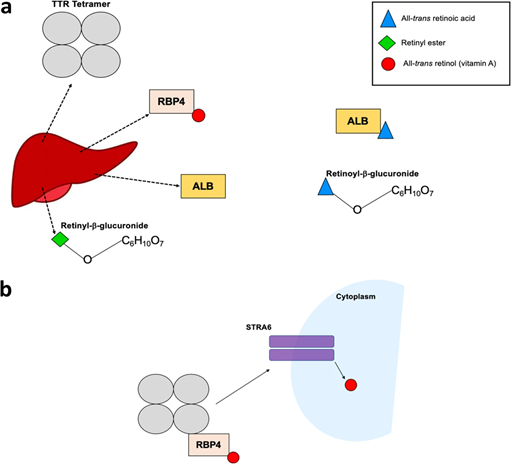 مخطط يوضح آلية نقل الريتينويد جهازيًا[/caption]
مخطط يوضح آلية نقل الريتينويد جهازيًا[/caption]
توجد ثلاثة تصنيفات لحمض الريتينويد باعتباره رابطًا :
- مستقبلات حمض الريتينويك retinoic acid receptors (RAR)
- مستقبلات الريتينويد إكس retinoid X receptors (RXR)
- مستقبلات بيروكسيسوم المنشطة بيتا ودلتا peroxisome proliferator-activated receptor beta/delta (PPARβ/δ)
(ولكل من RAR وRXR ثلاثة أنواع فرعية: ألفا وبيتا وغاما).
وترتبط هذه المستقبلات مع الحمض النووي في تتابعات مميزة، تُسمى عناصر استجابة حمض الريتينويك retinoic acid response elements (RARE).
التعبير الجيني لاضطراب تنظيم الريتينويدات في الفصام
كانت مشكلة دراسات الجينوم الأولى لمرض الفصام أن عيناتها كانت صغيرة الحجم، واعتمدت على طرق الارتباط لتحديد الجينات المسؤولة.
يمكن تحديد الرابط بين الواسم الجيني Genomic Marker والنمط الظاهري Phenotype، عن طريق اختبار (genome-wide association studies) أو اختصارًا (GWAS)، كشف هذا الاختبار في مرضى الفصام وجود نحو 150 موضع جيني يرتبط بالفصام بوضوح، 5 من هذه المسارات متعلق بجينات ترتبط بتصنيع وتنظيم الريتينويدات، إضافةً لأنظمة أخرى مهمة في الطبيعة المرضية للفصام مثل الإشارات الدوبامينية والجلوتاميرية.
وقد وُجد أن أكثر الواسمات الجينية أهمية هو الموجود بداخل جين RERE (arginine-glutamic acid dipeptide repeats)، الذي من وظائفه تشفير عائلة بروتين الأتروبين، وقد أثبت اختبار GWAS دور هذا الجين في أمراض أخرى مثل الاكتئاب والتهاب الأعصاب.
تغير التعبير عن نسخ الريتينويدات في مرض الفصام
أثبتت تحاليل التعبير الجيني دور الريتينويدات في الطبيعة المرضية للفصام، وكشفت المتابعات التي أجريت مؤخرًا لعينات القشرة الدماغية بعد الوفاة في أكثر من 500 حالة فصام وجود اختلاف في التعبير عن جينات مسار الريتينويدات، ولكن التتابع RARE ينظم آلاف عمليات الاستنساخ، لذلك فإن ارتباط المرض جينيًا بـRARE لا يُعَد دليلًا مباشرًا على دور الريتينويدات في المرض، ومع ذلك فإن الجينات التي ينظمها RARE قد تنتج آليات يكون فيها خلل الريتينويد ضمن أسباب الفصام.
التدخلات السريرية التي تستهدف نظام الريتينويد في مرض الفصام
تشير البيانات إلى فائدة العلاجات القائمة على الريتينويدات في الممارسة السريرية، وترجع أهمية استهداف الريتينويدات علاجيًا إلى إمكانية تعديل النظام عن طريق التدخل الغذائي، ومن المثير للاهتمام أنه قد ثبت انخفاض تركيز البيتاكاروتين Beta-Carotene عند بعض مرضى الفصام، إضافةً إلى إمكانية التدخل المباشر بإعطاء أدوية تعمل على تنشيط مستقبلات الريتينويد.
تشير نتائج تجربتين سريريتين منفصلتين إلى فاعلية ناهضات RXR الصناعية مثل البيكساروتين Bexarotene في علاج الفصام، وقد أظهرت الجرعات المنخفضة من العلاج تحملًا جيدًا، وتحسنًا ملحوظًا باعتبار مقياس الأعراض الإيجابية والسلبية (PANSS) للنتائج الأولية.
وإن كنا في حاجة إلى المزيد من التجارب للتأكد من سلامة وفاعلية هذا التدخل، ويجب الأخذ في الحسبان عند إجراء التجارب السريرية وجود أنماط جينية تشفر مستقبلات RXR ، فيمنع الاختلاف الناتج ارتباط المركب بالمستقبِل، ولا يستطيع المريض الاستفادة من البيكساروتين.
الخلاصة أنه من المهم إجراء المزيد من التجارب السريرية باستخدام مركبات الريتينويد للتأكد من فاعليتها في علاج حالات الفصام، وقد يقدم التدخل الجيني في هذه التجارب حلًا واعدًا لمشكلة صعوبة الاستفادة السريرية الصحيحة.
اقرأ أيضًا:
اكتشاف طريقة جديدة للكشف المبكر عن الفصام قبل ظهور الأعراض!
ترجمة: ولاء سليمان
تدقيق: أكرم محيي الدين
مراجعة: صهيب الأغبري
الكاتب
ولاء سليمان
